Sintomi e diagnosi ma anche gli aspetti meno noti della malattia di Lyme: ceppi batterici, diagnosi, ospiti serbatoio, controversie e ricerca scientifica in corso
La borreliosi di Lyme è un’infezione batterica che si trasmette all’uomo attraverso il morso di zecche appartenenti alla famiglia Ixodes. Il batterio responsabile è tipicamente Borrelia burgdorferi negli Stati Uniti, mentre in Europa e in Asia entrano in gioco anche altri ceppi, come B. afzelii e B. garinii. Questa patologia è considerata una delle zoonosi più diffuse nelle regioni temperate dell’emisfero settentrionale, in particolare durante le stagioni più calde, quando le zecche sono attive.
La borreliosi di Lyme rappresenta una minaccia sanitaria concreta, ma affrontabile. Conoscere i sintomi, agire rapidamente e adottare misure preventive può fare la differenza nel ridurre le complicanze. Il riconoscimento precoce della malattia e un trattamento tempestivo restano fondamentali per garantire un buon recupero clinico
Sintomi e Contagio
Il passaggio dell’infezione avviene quando una zecca infetta si attacca alla pelle umana e rimane ancorata abbastanza a lungo da trasmettere il microrganismo. Le zecche si infettano nutrendosi del sangue di animali selvatici, spesso roditori, uccelli o cervi, che fungono da serbatoio naturale della Borrelia.
🩺 Sintomi della Malattia di Lyme:
| Sintomo | Frequenza stimata | Note |
|---|---|---|
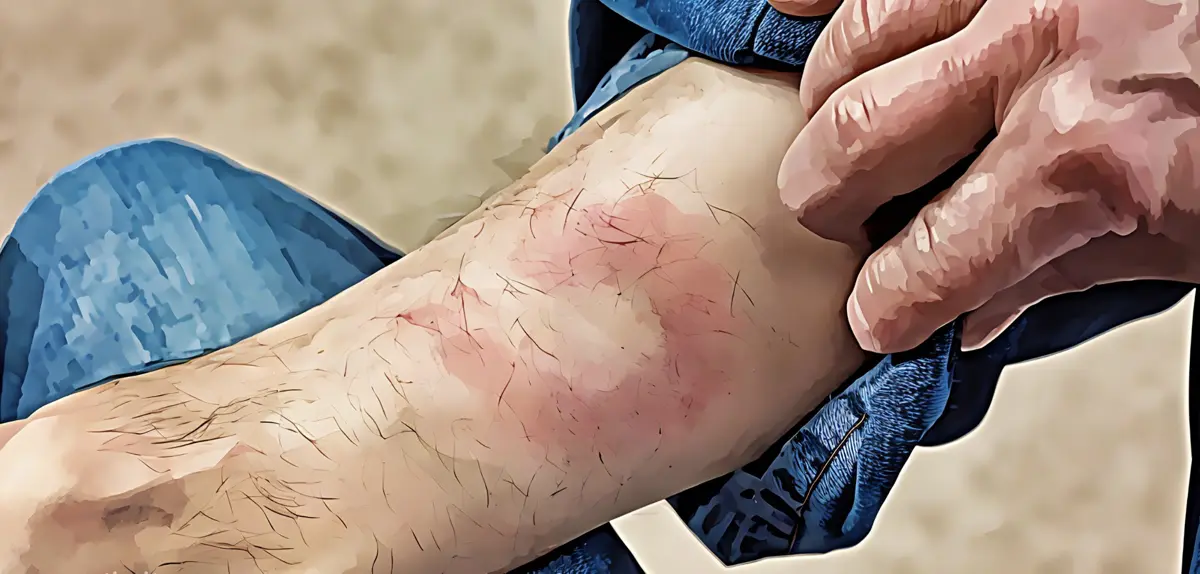
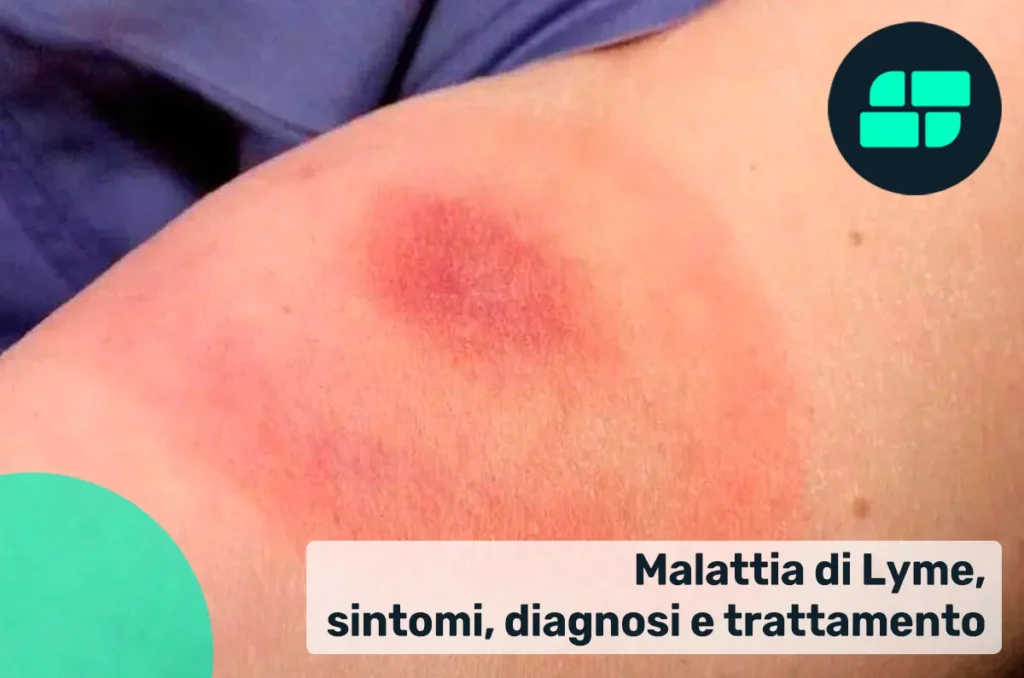
| Eritema migrante | 70–80 % | Lesione cutanea tipica, spesso a “bersaglio” |
| Febbre, brividi, mal di testa, affaticamento, dolori muscolari/articolari | Molto comuni | Sintomi simil-influenzali |
| Linfoadenopatia | Comuni | Linfonodi ingrossati |
| Eritemi migranti multipli | 10–20 % nei casi non trattati | Disseminazione cutanea |
| Mal di testa intenso e rigidità nucale | Più frequenti nelle fasi disseminate | Segni di neuroborreliosi |
| Paralisi facciale (Bell’s palsy) | 5–15 % nei casi non trattati | Segno neurocardiale |
| Artrite ricorrente, soprattutto alle ginocchia | ~25 % dei casi segnalati | Gonfiore e dolori articolari |
| Dolori tendinei, muscolari, ossei intermittenti | Comuni | Sintomi muscolo-scheletrici |
| Palpitazioni, aritmia, sensazione di giramento di testa | 4–10 % | Carditi da Lyme |
| Nervo radicolare e neuropatie periferiche (dolore, torpore) | Comuni nelle fasi disseminate | Radiculopatia e neuropatia |
| Linfo-citi meningite, encefalite, mielite | Meno frequenti | Coinvolgimento CNS |
| Acrodermatite cronica atrofica | Rara (Europa) | Manifestazione cutanea cronica |
| Sequele neuropsichiatriche: atassia, convulsioni, corea, disfasia | Rari | Neuroborreliosi cronica |
| Disturbi cognitivi, problemi di memoria, affaticamento persistente | 10–20 % dopo terapia (PTLDS) | Sindrome post-trattamento |
L’uomo rappresenta un ospite accidentale nel ciclo di vita del parassita.
La Borrelia ha una particolare affinità per articolazioni, tessuto cardiaco e sistema nervoso centrale e periferico, dove può causare manifestazioni multiorgano.
- Fase iniziale (localizzata)
I primi segnali possono comparire entro un intervallo che va da pochi giorni fino a un mese dopo il morso. Il segno clinico più caratteristico è l’eritema migrante, una lesione cutanea che si allarga progressivamente e che può assumere la forma di un anello o di un bersaglio. Si associano frequentemente sintomi simil-influenzali: spossatezza, febbre, dolori articolari e cefalea. Dopo il morso della zecca, la Borrelia penetra nella cute e inizia a replicarsi nel tessuto sottocutaneo. Grazie alla sua forma a spirale (spirocheta) e a speciali proteine superficiali, riesce a muoversi attraverso la matrice extracellulare e a eludere il sistema immunitario nelle prime fasi dell’infezione. - Fase disseminata precoce
Nel giro di settimane, il batterio può diffondersi ad altri distretti corporei attraverso il sangue, determinando la comparsa di sintomi sistemici. Tra questi si includono disturbi neurologici come la paralisi del nervo facciale, alterazioni del ritmo cardiaco (come la blocco atrioventricolare) e infiammazioni muscolo-articolari. In assenza di trattamento, il batterio riesce a entrare nel flusso sanguigno (batteriemia) e a colonizzare diversi organi e tessuti. - Fase tardiva
Se l’infezione non viene diagnosticata e trattata tempestivamente, può evolvere in forme croniche che includono artrite persistente, problemi neurologici più severi (come encefalopatie) o infiammazioni del cuore.
Diagnosi
L’iter diagnostico inizia con un’attenta valutazione clinica e anamnestica: l’eventuale esposizione a zone infestate da zecche, la presenza del tipico eritema migrante, e la sintomatologia associata. La conferma di laboratorio si ottiene mediante test sierologici in due fasi: un primo screening con il test ELISA, seguito, in caso di positività, dalla conferma tramite Western blot ma i test sierologi non sono infallibili. L’organismo inizia a produrre anticorpi rilevabili solo dopo diversi giorni dall’infezione, rendendo difficile una diagnosi immediata. Inoltre, è possibile riscontrare:
- falsi negativi nelle fasi iniziali;
- falsi positivi dovuti a reazioni con altri patogeni, come ad esempio il virus di Epstein-Barr o i batteri della sifilide.
Per questi motivi, la valutazione clinica, unita all’osservazione dei sintomi e alla verifica di possibili esposizioni alle zecche, rimane un elemento insostituibile nel processo diagnostico.
| Aspetto | Meccanismo fisiopatologico principale |
|---|---|
| Infezione iniziale | Invasione cutanea e moltiplicazione locale |
| Disseminazione | Diffusione ematica verso altri organi |
| Infiammazione sistemica | Risposta immunitaria che può danneggiare i tessuti |
| Persistenza cronica | Evasione immunitaria, biofilm, localizzazione in tessuti profondi |
| Complicanze tardive | Artrite, neuroborreliosi, disturbi cardiaci |
In risposta all’infezione da Borrelia, si attivano sia i meccanismi dell’immunità innata (coinvolgendo cellule come macrofagi e neutrofili, oltre a citochine pro-infiammatorie), sia quelli dell’immunità adattativa, con la produzione sequenziale di anticorpi IgM e IgG. La risposta si rivela spesso incompleta, soprattutto nelle fasi avanzate, favorendo l’instaurarsi di fenomeni infiammatori cronici e danni autoimmunitari, in particolare a livello articolare.
Terapia
Se riconosciuta nei primi stadi, la malattia è solitamente risolvibile con antibiotici orali, come doxiciclina o amoxicillina, assunti per alcune settimane. La prognosi è favorevole nella maggior parte dei casi. Una parte dei pazienti può accusare una persistenza dei sintomi anche dopo la cura, condizione definita come sindrome post-trattamento della malattia di Lyme (PTLDS), che si manifesta con stanchezza cronica, dolori muscolari o deficit cognitivi.
🧩 Complicanze e patologie correlate:
| Complicanza / Patologia | Descrizione |
|---|---|
| Neuroborreliosi | Coinvolgimento del sistema nervoso con meningite linfocitaria, neuriti craniche, radicoliti, neuropatie periferiche; possibili encefalite e mielite nelle forme tardive (en.wikipedia.org) |
| Lyme carditis | Infiammazione cardiaca con blocco atrioventricolare, palpitazioni, svenimenti; in 0,3–10 % dei casi |
| Artrite di Lyme | Infiammazione delle grandi articolazioni, spesso ginocchia, con episodi recidivanti; possibile danno articolare permanente |
| Acrodermatite cronica atrofica | Lesione cutanea cronica, con deterioramento della pelle e perdita di peli (Europa) |
| Sindrome post-trattamento di Lyme (PTLDS) | Persistenza di affaticamento, dolore muscoloscheletrico, cefalea e disturbi cognitivi dopo terapia antibiotica, in 10–20 % dei pazienti |
| Manifestazioni neurologiche tardive gravi | Atassia, convulsioni, chorea, disfasia, paralisi cronica da neuroborreliosi tardiva |
| Neuropatia periferica cronica | Dannigio nervoso a lungo termine, con parestesie o anestesia |
La malattia di Lyme presenta una distribuzione eterogenea a livello europeo. In alcune aree il numero di casi è relativamente contenuto, con un’incidenza intorno ai 20 casi ogni 100.000 abitanti, mentre in regioni ad alta endemia, come alcune zone della Scandinavia – in particolare la Finlandia – i tassi possono superare i 500 casi ogni 100.000 abitanti.
A livello globale, la borreliosi è diffusa principalmente nelle aree a clima temperato dell’emisfero nord. I cambiamenti climatici e l’innalzamento delle temperature medie stanno ampliando progressivamente l’areale delle zecche vettori, favorendo la comparsa della malattia in nuove aree e rendendola una problematica sanitaria di rilievo internazionale.
Per contenere il rischio di infezione è opportuno adottare comportamenti protettivi, soprattutto durante attività all’aperto in ambienti boschivi o erbosi. Tra le misure suggerite figurano:
- evitare il contatto diretto con vegetazione fitta, come erba alta e cespugli;
- applicare repellenti per insetti contenenti sostanze attive riconosciute come efficaci (es. DEET o permetrina);
- indossare abiti coprenti e di colore chiaro, che facilitino l’individuazione delle zecche;
- ispezionare accuratamente il corpo al rientro da ambienti a rischio e rimuovere immediatamente eventuali zecche, seguendo procedure corrette di estrazione con l’ausilio di pinzette.
Sebbene la malattia di Lyme sia ormai nota in ambito medico per le sue cause, i sintomi e le principali complicazioni, esistono ancora elementi meno discussi che completano il quadro clinico e scientifico della patologia. Approfondire questi aspetti consente di ottenere una comprensione più articolata e realistica del fenomeno, con importanti ricadute sia sul piano della diagnosi che della gestione del paziente.
Contrariamente a quanto si possa pensare, l’infezione da Lyme non è provocata da un solo tipo di microrganismo, bensì da un gruppo di batteri appartenenti al complesso Borrelia burgdorferi sensu lato.
Nel continente americano, il principale agente infettivo è B. burgdorferi sensu stricto, mentre in Europa e in alcune zone asiatiche sono implicati anche B. afzelii, B. garinii e B. spielmanii.
Ciascuna di queste varianti può produrre effetti clinici differenti: alcune tendono a colpire la pelle, altre il sistema nervoso o l’apparato articolare. Questo spiega perché i sintomi e le manifestazioni della malattia variano sensibilmente a seconda dell’area geografica e del ceppo coinvolto.
Le zecche, principali vettori della malattia, si infettano nutrendosi del sangue di animali che fungono da riserva del batterio.
Tra i più importanti serbatoi naturali si annoverano:
- piccoli roditori, come i topi selvatici (Peromyscus leucopus) in America del Nord;
- diverse specie di uccelli;
- cervi, i quali, pur non trasmettendo direttamente il patogeno, sono essenziali per la riproduzione delle zecche.
La comprensione di questa catena ecologica è cruciale per lo sviluppo di strategie ambientali di prevenzione e contenimento della diffusione della Borrelia.
Un tema ancora controverso riguarda l’ipotesi di una forma cronica dell’infezione. Alcuni pazienti continuano a lamentare sintomi debilitanti — come stanchezza persistente, dolori diffusi o difficoltà cognitive — anche dopo una terapia antibiotica adeguata.
La comunità scientifica riconosce questa condizione come sindrome post-trattamento di Lyme (PTLDS), ma non vi sono prove certe che indichino la presenza attiva e continuativa del batterio nell’organismo. La discussione resta aperta, con studi in corso per chiarire l’origine e la natura di questi disturbi persistenti.
L’impatto della Lyme sulla vita delle persone può essere significativo, soprattutto nei casi in cui la diagnosi sia tardiva o il trattamento inefficace.
Questo si traduce in un aumento dei costi per il sistema sanitario e in un peso psicologico notevole per i pazienti. Inoltre, la scarsa informazione diffusa tra la popolazione generale e anche tra alcuni operatori sanitari può rallentare l’intervento precoce e contribuire alla sottovalutazione della patologia.
Diversi ambiti di studio sono attualmente in evoluzione:
- la sperimentazione di vaccini specifici destinati all’uomo;
- lo sviluppo di metodi diagnostici più precoci e affidabili;
- l’indagine dei meccanismi immunologici che consentono al batterio di eludere le difese dell’ospite;
- la comprensione più approfondita dei fattori che determinano la comparsa della sindrome post-trattamento.
Queste ricerche potrebbero, in futuro, migliorare sia la prevenzione sia la qualità della cura per i pazienti colpiti da questa complessa malattia infettiva.