Artrite psoriasica, panoramica completa su sintomi, cause, comorbidità e trattamenti farmacologici e non farmacologici basati su evidenze scientifiche aggiornate
L’artrite psoriasica (PsA) è una forma cronica di infiammazione articolare associata alla psoriasi. Generalmente, colpisce tra lo 0,1 % e lo 0,2 % della popolazione nel mondo. Tuttavia, tra chi soffre di psoriasi cutanea, si riscontra in circa 15–30 % dei casi, con la sintomatologia cutanea che precede quella articolare nel 70 % dei pazienti.
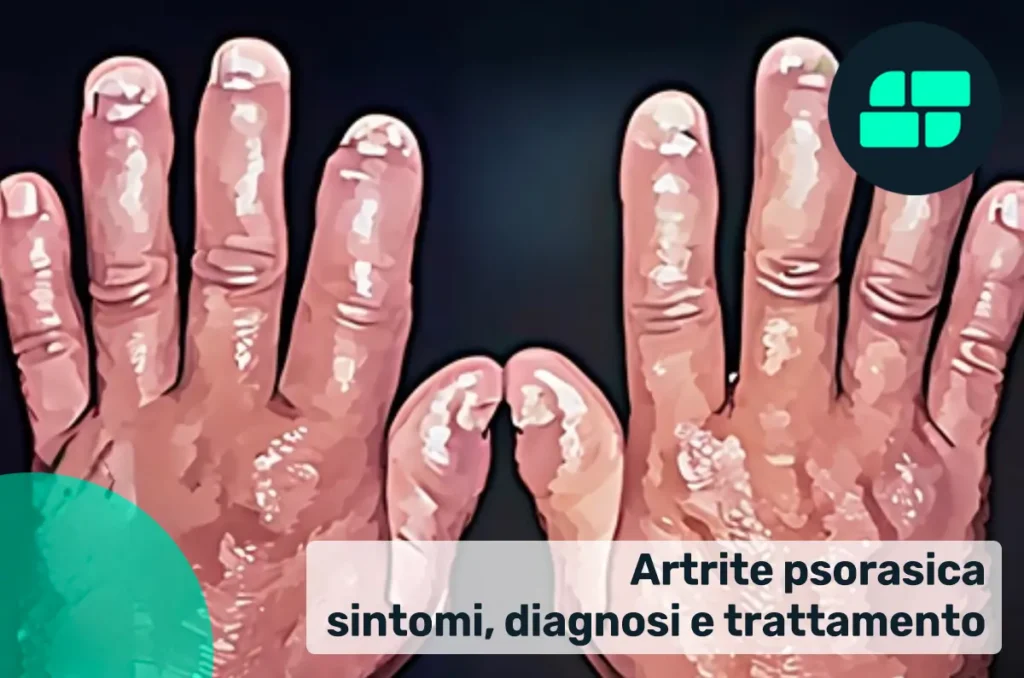
L’artrite psoriasica (PsA) è una malattia infiammatoria cronica delle articolazioni che si manifesta in individui con psoriasi, spesso con un ritardo diagnostico importante
Le sue radici risiedono in una complessa combinazione tra predisposizione genetica, alterazioni del sistema immunitario e fattori ambientali scatenanti. In particolare, le cellule immunitarie chiamate Th17 e la citochina TNF‑alfa ricoprono un ruolo cruciale nell’innesco e nel mantenimento dell’infiammazione, contribuendo a danneggiare le articolazioni e ad alimentare l’infiammazione delle entesi, ovvero i punti in cui tendini e legamenti si inseriscono sull’osso.
Nelle fasi iniziali dell’artrite psoriasica, prima che si manifestino i sintomi clinici, può verificarsi una disfunzione immunitaria in soggetti predisposti geneticamente. Questa fase silente è caratterizzata da un’attivazione anomala del sistema immunitario in risposta a stimoli ambientali come infezioni, microtraumi o stress meccanici. Le cellule del sistema immunitario innato, come monociti e cellule dendritiche, si attivano in particolare nei punti di inserzione di tendini e legamenti sull’osso (le entesi), dando avvio a una cascata infiammatoria.
In questo contesto vengono prodotte molecole infiammatorie, come l’interleuchina-23 (IL-23), che stimolano una risposta immunitaria di tipo Th17. Tale risposta porta al rilascio di citochine proinfiammatorie tra cui IL‑17, IL‑22 e TNF‑α. Sebbene in questa fase non siano ancora presenti sintomi evidenti, questi segnali chimici alterano l’ambiente locale e preparano l’organismo alla fase infiammatoria conclamata.
Con la progressione della malattia, si verifica un’intensificazione della risposta immunitaria. Le citochine infiammatorie guidano l’accumulo di cellule immunitarie (neutrofili, macrofagi, linfociti T) nelle articolazioni periferiche e nelle entesi. Questo provoca infiammazione localizzata, con ispessimento del tessuto connettivo, microlesioni e attivazione delle cellule sinoviali. Tali cellule iniziano a produrre enzimi e mediatori responsabili del danno articolare. Inoltre, si attiva il sistema RANKL-RANK, che promuove la distruzione dell’osso da parte degli osteoclasti.
Clinicamente, questa fase si manifesta con gonfiore, dolore articolare e rigidità, soprattutto al mattino. Le prime erosioni ossee possono essere osservate solo mediante indagini diagnostiche ad alta sensibilità, come risonanza magnetica o ecografia con power Doppler.
Con il protrarsi dell’infiammazione, la malattia evolve in una fase di danno strutturale. L’infiltrato infiammatorio e le citochine promuovono l’erosione della superficie ossea e la rarefazione del tessuto subcondrale. Allo stesso tempo, meccanismi di riparazione aberranti innescati da molecole come le BMP e le prostaglandine determinano una ricostruzione disorganizzata dell’osso, con formazione di osteofiti e periostiti.
Il coinvolgimento cronico delle entesi può provocare cicatrici fibrotiche, calcificazioni e degenerazione tendinea. A livello della membrana sinoviale, la proliferazione patologica porta alla formazione del cosiddetto “panno sinoviale”, che invade la cartilagine articolare. Nei casi più avanzati, questo processo può condurre a una fusione delle articolazioni, di tipo fibroso o osseo, compromettendo gravemente la funzionalità articolare.
Nel processo patologico si attivano segnali molecolari complessi che includono mediatori come RANKL e BMP, nonché le prostaglandine, sostanze che orchestrano la distruzione e la rigenerazione dell’osso. Questo porta a due fenomeni contrapposti ma concomitanti: da una parte l’erosione del tessuto osseo e, dall’altra, la formazione di escrescenze anomale come osteofiti o periostiti, che alterano la struttura delle articolazioni.
Non va trascurata l’importanza dei sollecitamenti meccanici, soprattutto a livello delle entesi. Stress ripetuti o microtraumi possono scatenare o peggiorare l’infiammazione locale, specie in soggetti geneticamente predisposti. Questo contribuisce a spiegare perché alcune aree del corpo siano più frequentemente colpite, come talloni, gomiti o colonna vertebrale.
Per identificare correttamente questa condizione, si utilizzano i criteri CASPAR, un sistema diagnostico che richiede l’evidenza di un’artrite associata ad almeno tre dei seguenti elementi: presenza o storia di psoriasi cutanea, lesioni ungueali tipiche, gonfiore diffuso delle dita (dattilite), radiografie che mostrano caratteristiche peculiari della malattia e assenza del fattore reumatoide. Questo insieme di parametri consente ai clinici di distinguere la PsA da altre malattie reumatiche in modo preciso.
| Strumento / Test | Descrizione | Scopo Principale | Fonte |
|---|---|---|---|
| Criteri CASPAR | Sistema di classificazione basato su manifestazioni cliniche e radiografiche | Diagnosi e classificazione | PubMed |
| DAPSA | Indice che valuta attività articolare tramite parametri clinici e laboratoristici | Monitoraggio attività della malattia | Arthritis Care Res |
| PASDAS | Valutazione complessiva dello stato di malattia articolare e cutanea | Monitoraggio globale | PubMed |
| PASI | Valutazione gravità della psoriasi cutanea | Monitoraggio psoriasi | DermNet NZ |
| PCR e VES | Marker di infiammazione generica | Valutazione infiammazione | Mayo Clinic |
| Fattore Reumatoide e Anti-CCP | Test per differenziare PsA da artrite reumatoide | Diagnosi differenziale | Arthritis Foundation |
| HLA-B27 | Marker genetico associato all’artrite assiale | Supporto diagnostico in PsA assiale | NIH |
| Ecografia articolare | Imaging per valutare infiammazione, entesiti e danni articolari | Diagnosi precoce e monitoraggio | EULAR |
| Risonanza magnetica (RM) | Imaging sensibile per lesioni infiammatorie precoci e danni articolari | Diagnosi e monitoraggio | RadiologyInfo |
| Rx tradizionale | Valutazione danni ossei e proliferazioni ossee tipiche | Valutazione danno strutturale | Radiopaedia |
| Linee guida EULAR/GRAPPA/ACR | Raccomandazioni per diagnosi e gestione della PsA | Supporto clinico e terapeutico | EULAR, GRAPPA, ACR |
L’artrite psoriasica è spesso accompagnata da una serie di patologie concomitanti che ne influenzano il decorso e la gestione clinica. Le condizioni più frequentemente associate possono essere suddivise in quattro principali gruppi: cardiovascolari, metaboliche, infiammatorie/autoimmuni e psichiche.
Nel primo gruppo rientrano le malattie cardiovascolari, tra cui l’ipertensione arteriosa, molto comune tra i pazienti affetti. Sono frequenti anche la cardiopatia ischemica, lo scompenso cardiaco e l’aterosclerosi precoce, tutti legati a uno stato infiammatorio cronico sistemico. Inoltre, il rischio di eventi tromboembolici risulta aumentato a causa di alterazioni nella funzione endoteliale e della coagulazione.

L’artrite psoriasica è una patologia sistemica che richiede un’attenzione accurata sia per le sue manifestazioni articolari che per le possibili complicanze a livello sistemico. La sua complessità impone un approccio integrato e personalizzato, capace di affrontare la molteplicità delle sue forme cliniche e delle condizioni concomitanti. L’adozione tempestiva di criteri diagnostici come quelli CASPAR, unita alla disponibilità di terapie innovative, consente oggi una gestione più efficace rispetto al passato, migliorando significativamente la prognosi e il benessere dei pazienti
I disturbi metabolici rappresentano un altro ambito rilevante. Tra questi figurano la sindrome metabolica, l’obesità e la dislipidemia, spesso caratterizzata da alti livelli di trigliceridi e riduzione del colesterolo HDL. Anche il diabete mellito di tipo 2 è frequente, favorito dalla resistenza insulinica causata dall’infiammazione cronica. A queste condizioni si aggiunge spesso la steatosi epatica non alcolica, generalmente correlata al sovrappeso e alla stessa infiammazione sistemica.
Sul piano immunologico e infiammatorio, la PsA può coesistere con malattie infiammatorie croniche dell’intestino, come il morbo di Crohn e la colite ulcerosa, oppure con uveiti, ossia infiammazioni oculari che possono colpire entrambi gli occhi. Anche l’osteoporosi può svilupparsi, spesso come risultato di inattività, infiammazione persistente e uso prolungato di corticosteroidi. In alcuni casi è stata rilevata anche un’associazione con la malattia celiaca.
Non vanno trascurati i disturbi psichici e neurocomportamentali. L’ansia e la depressione sono particolarmente diffuse e incidono negativamente sulla qualità della vita. I disturbi del sonno sono comuni e possono essere causati dal dolore cronico e dall’infiammazione. In stadi avanzati della malattia, è stato ipotizzato un possibile declino cognitivo, attribuito al prolungato stato infiammatorio sistemico.
| Categoria | Patologia associata | Prevalenza stimata / Note | Tipo di correlazione |
|---|---|---|---|
| Cardiovascolare | Ipertensione arteriosa | ~34% | Conseguenza/associazione infiammatoria |
| Aterosclerosi precoce / cardiopatia ischemica | 19–43% | Conseguenza dell’infiammazione cronica | |
| Tromboembolia venosa / arteriosa | Non quantificata, rischio aumentato | Conseguenza | |
| Metabolica | Sindrome metabolica | ~29% | Conseguenza e fattore aggravante |
| Obesità | 27–29% | Fattore di rischio e amplificatore | |
| Dislipidemia | ~24% | Conseguenza dell’infiammazione | |
| Diabete mellito tipo 2 | Elevato rischio | Conseguenza | |
| Steatosi epatica non alcolica (NAFLD) | Frequente ma non sempre diagnosticata | Conseguenza | |
| Autoimmuni / Infiammatorie | Malattie infiammatorie intestinali (IBD) | Fino al 10–15% | Associazione genetica/immunitaria |
| Uveite anteriore | Episodi ricorrenti, anche bilaterali | Manifestazione associata | |
| Osteoporosi | Variabile, aumentata dal disuso e da farmaci | Conseguenza | |
| Malattia celiaca | Rara, ma documentata in co-occorrenza | Associazione autoimmune | |
| Psichiche / Neurologiche | Ansia e depressione | Molto frequenti (>30%) | Conseguenza multifattoriale |
| Insonnia e disturbi del sonno | Comuni | Conseguenza | |
| Compromissione cognitiva lieve | Non confermata, ma ipotizzata in malattia avanzata | Possibile conseguenza indiretta |
Sintomi
Il quadro clinico può variare considerevolmente tra i pazienti. Alcuni presentano un’artrite asimmetrica che interessa poche articolazioni (oligoartrite), mentre altri sviluppano una forma simmetrica e diffusa (poliartrite). Un’altra forma coinvolge principalmente la colonna vertebrale, detta spondilite psoriasica. Spesso si osservano anche dattilite (dita tumefatte a forma di salsicciotto), entesiti e modificazioni a carico delle unghie.
L’artrite psoriasica non è rara, ma spesso passa inosservata: circa quattro casi su dieci potrebbero sfuggire alla diagnosi. Le stime indicano una frequenza annuale compresa tra 6 e 35 nuovi casi ogni 100.000 persone.
| Sintomo/Manifestazione | Frequenza (%) | Meccanismo e Implicazioni cliniche |
|---|---|---|
| Artrite periferica | Olgioarticolare → ~70%Simmetrica → ~15% | Infiammazione sinoviale con tumefazione, dolore, rigidità mattutina; può causare erosioni sequenziali in assenza di terapia |
| Dattilite | ~40% | Coinvolgimento sinoviale, entesi e tenosinoviale che causa tumefazione uniforme del dito |
| Enthesites | 19–65 % (media ~40 %) | Infiammazione dei siti di inserzione tendinea/legamentosa (es. Achille, pianta del piede); correlata con attività più aggressiva della malattia |
| Coinvolgimento assiale | 25–70 % | Dolore e rigidità vertebrale, sacro-iliite, migliora col movimento; può progredire verso fusione vertebrale |
| Alterazioni ungueali | ~60 % | Pit‑ting, onicolisi, “oil drop”, subungual hyperkeratosis; indicatore utile di malattia sistemica attiva |
| Uveite | ~3–4 % | Infiammazione oculare anteriore, dolorosa, possibile implicazione visiva |
| Malattie infiammatorie intestinali | ~3 % | Manifestazione extra-articolare, condivisa nei meccanismi immunitari |
| Affaticamento (fatigue) | ~30 % | Sintomo sistemico, correlato a infiammazione cronica e disturbi del sonno |
Uno dei primi segni è il coinvolgimento delle articolazioni periferiche, in particolare di dita, mani, polsi, ginocchia e caviglie. Queste articolazioni possono risultare dolenti, gonfie e rigide, soprattutto al risveglio. La presentazione è spesso asimmetrica e interessa poche articolazioni (oligoartrite), anche se in una parte dei casi può avere una distribuzione simmetrica.
Un’altra manifestazione tipica è la dattilite, nota anche come “dito a salsicciotto”, in cui un intero dito della mano o del piede si presenta gonfio e dolente per l’infiammazione simultanea di tendini, articolazioni e tessuti molli. Questa condizione si osserva in circa il 40% dei pazienti.
Un sintomo frequente è rappresentato anche dall’entesite, ovvero l’infiammazione nei punti in cui tendini e legamenti si inseriscono sull’osso. Le sedi più colpite sono il tallone (tendine d’Achille), la pianta del piede, il ginocchio e la spalla. Questa manifestazione può interessare fino al 65% dei pazienti.
Il coinvolgimento assiale, ovvero delle articolazioni vertebrali e sacro-iliache, si traduce in dolore lombare e rigidità, che tendono a migliorare con il movimento. È un quadro tipico delle artriti infiammatorie e può comparire in una percentuale significativa di pazienti.
Anche le alterazioni delle unghie rappresentano una componente caratteristica della malattia. Queste comprendono piccole depressioni puntiformi (pitting), sollevamento dell’unghia dal letto (onicolisi), ispessimento e discromie simili a macchie d’olio. La malattia può coinvolgere anche distretti extra-articolari, con manifestazioni come uveite anteriore, un’infiammazione dell’occhio che può compromettere la vista, e malattie infiammatorie intestinali come il morbo di Crohn e la colite ulcerosa, seppur meno frequenti.
È anche comune la comparsa di affaticamento cronico, una sensazione persistente di stanchezza, spesso legata al dolore continuo e ai disturbi del sonno associati alla condizione infiammatoria.
Cura
Sebbene non esista ancora una cura risolutiva, oggi sono disponibili numerose terapie che mirano a spegnere l’infiammazione e a contenere il danno articolare, con l’obiettivo finale di migliorare la qualità della vita del paziente. Le opzioni includono:
- Farmaci antinfiammatori non steroidei (FANS), utilizzati per brevi periodi in forme leggere
- DMARD convenzionali, come il metotrexato, efficaci nei casi con interessamento periferico
- Terapie biologiche, tra cui gli inibitori del TNF (come il certolizumab) e gli antagonisti delle interleuchine IL‑17 e IL‑23 (es. secukinumab, bimekizumab, ustekinumab, risankizumab)
La selezione del trattamento avviene sulla base di diversi fattori: gravità dei sintomi, presenza di comorbidità, preferenze del paziente e sicurezza dei farmaci. L’approccio ideale è quello del “decision making condiviso”, che prevede un dialogo continuo tra medico e paziente, guidato da protocolli clinici e dal metodo GRADE per valutare la solidità delle evidenze scientifiche.
Terapie farmacologiche:
| Categoria terapeutica | Principali farmaci / meccanismi | Indicazioni principali | Meccanismo d’azione | Note scientifiche |
|---|---|---|---|---|
| FANS (Farmaci anti-infiammatori non steroidei) | Ibuprofene, naprossene, diclofenac | Gestione sintomi lievi-moderati | Inibizione della cicloossigenasi (COX), riduzione delle prostaglandine infiammatorie | Utilizzati a breve termine per controllo del dolore e infiammazione; non modificano il decorso della malattia |
| DMARD tradizionali (farmaci antireumatici modificanti la malattia) | Metotrexato, sulfasalazina, leflunomide | Artrite periferica, soprattutto oligo- e poliarticolare | Soppressione delle risposte immunitarie aberranti, effetti immunomodulanti | Metotrexato è il più usato, migliora sintomi articolari e cutanei, ma non sempre efficace su entesite o assiale |
| Biologici anti-TNFα | Etanercept, infliximab, adalimumab, certolizumab | Forme moderate-severe con coinvolgimento articolare e cutaneo | Blocco del TNFα, citochina pro-infiammatoria centrale nella PsA | Efficaci nel ridurre infiammazione, migliorano anche entesite e manifestazioni cutanee |
| Biologici anti-IL-17 | Secukinumab, ixekizumab, bimekizumab | Forme attive con coinvolgimento articolare e cutaneo | Inibizione di IL-17, citochina chiave nella risposta infiammatoria e distruzione tissutale | Utilizzati anche in pazienti non responsivi a anti-TNF |
| Biologici anti-IL-12/23 e anti-IL-23 | Ustekinumab, risankizumab | PsA con importante componente cutanea e articolare | Blocco delle citochine IL-12 e IL-23, coinvolte nella regolazione delle cellule Th17 | Possono modulare la risposta immunitaria più a monte rispetto a anti-IL-17 |
| Inibitori JAK | Tofacitinib, upadacitinib | Forme moderate-severe refrattarie a DMARD e biologici | Blocco delle chinasi JAK, che mediano segnali infiammatori intracellulari | Farmaci orali con efficacia su diversi aspetti della PsA, ma con necessità di monitoraggio per effetti collaterali |
| Corticosteroidi | Prednisone, metilprednisolone | Uso limitato, spesso in casi di riacutizzazioni | Potenti anti-infiammatori e immunosoppressori | Non consigliati a lungo termine per il rischio di effetti collaterali e osteoporosi |
Approcci non farmacologici:
| Intervento | Descrizione | Benefici scientificamente documentati | Note |
|---|---|---|---|
| Fisioterapia e esercizio fisico | Programmi personalizzati di esercizio, stretching, potenziamento muscolare | Miglioramento della mobilità articolare, riduzione della rigidità e del dolore, mantenimento della funzionalità | Fondamentale per prevenire l’atrofia muscolare e l’anchilosi |
| Terapia occupazionale | Adattamento delle attività quotidiane e utilizzo di ausili | Migliora la qualità della vita riducendo lo stress sulle articolazioni | Supporta l’autonomia e riduce il rischio di danni articolari |
| Educazione terapeutica | Informazione sul decorso della malattia e gestione delle terapie | Favorisce l’aderenza alle cure e il coping con la malattia | Importante per la collaborazione medico-paziente |
| Dieta e controllo del peso | Alimentazione bilanciata, gestione dell’obesità | Riduce l’infiammazione sistemica e il carico sulle articolazioni | L’obesità è fattore di rischio per peggioramento della PsA |
| Gestione dello stress e supporto psicologico | Strategie per affrontare ansia, depressione e fatica | Migliora il benessere generale e la qualità di vita | Considerato parte integrante della cura multidisciplinare |
La ricerca dedicata continua a progredire rapidamente, guidata dall’obiettivo di affinare la diagnosi precoce, sviluppare terapie sempre più su misura e approfondire la comprensione dei processi biologici alla base della malattia. I campi di innovazione più rilevanti comprendono la biotecnologia, la genetica, l’immunologia e nuove strategie terapeutiche emergenti.
Un traguardo fondamentale per il futuro è l’individuazione di biomarcatori precisi e affidabili, che permettano di differenziare la PsA da altre forme di artrite infiammatoria e, soprattutto, di prevederne l’insorgenza in soggetti con psoriasi cutanea. Le tecniche avanzate di analisi molecolare, come la proteomica, la metabolomica e lo studio dei microRNA, rappresentano strumenti promettenti per identificare segnali biologici precoci e specifici.
L’orientamento terapeutico si sta evolvendo verso un modello di medicina personalizzata, basata sulle caratteristiche genetiche e immunologiche individuali. Nuove classi di farmaci, inclusi i biologici di ultima generazione e gli inibitori di piccole molecole intracellulari — come i bloccanti delle vie JAK e i modulanti dell’interleuchina-23 — ampliano le opzioni terapeutiche disponibili, garantendo efficacia migliorata e ridotti effetti collaterali.
Emergenti ricerche evidenziano il ruolo potenziale del microbiota intestinale nel modulare la risposta immunitaria nella PsA. Questo suggerisce che interventi mirati a modificare il microbioma potrebbero diventare in futuro una strategia innovativa per gestire o prevenire la malattia. Le metodologie di imaging sono in costante sviluppo, con strumenti come la tomografia computerizzata ad alta risoluzione (HR-pQCT) e l’ecografia potenziata da nuove tecnologie, che permettono di individuare in modo sempre più tempestivo e preciso i danni articolari e le infiammazioni a livello delle entesi.
Il futuro trattamento della PsA si basa su un modello olistico e multidisciplinare, che integra farmaci, riabilitazione fisica, supporto psicologico e modifiche dello stile di vita. Questo approccio mira a migliorare non solo i sintomi della malattia, ma anche la qualità di vita complessiva e a ridurre le complicanze associate.